心不全分野
心不全は、予後不良な疾患群であり、新たな病態解明に基づいた治療法の開発が求められています。循環器内科学講座では、心不全の発症と進展の原因となる分子機構を解明するため、基礎研究から臨床研究まで一貫した取り組みを行っています。遺伝子・分子レベルから細胞、組織、そして個体レベルへと多階層的アプローチを行い、心不全の予防と治療開発につながる革新的なトランスレーショナル研究を目指しています。
1. 心不全と臓器連関
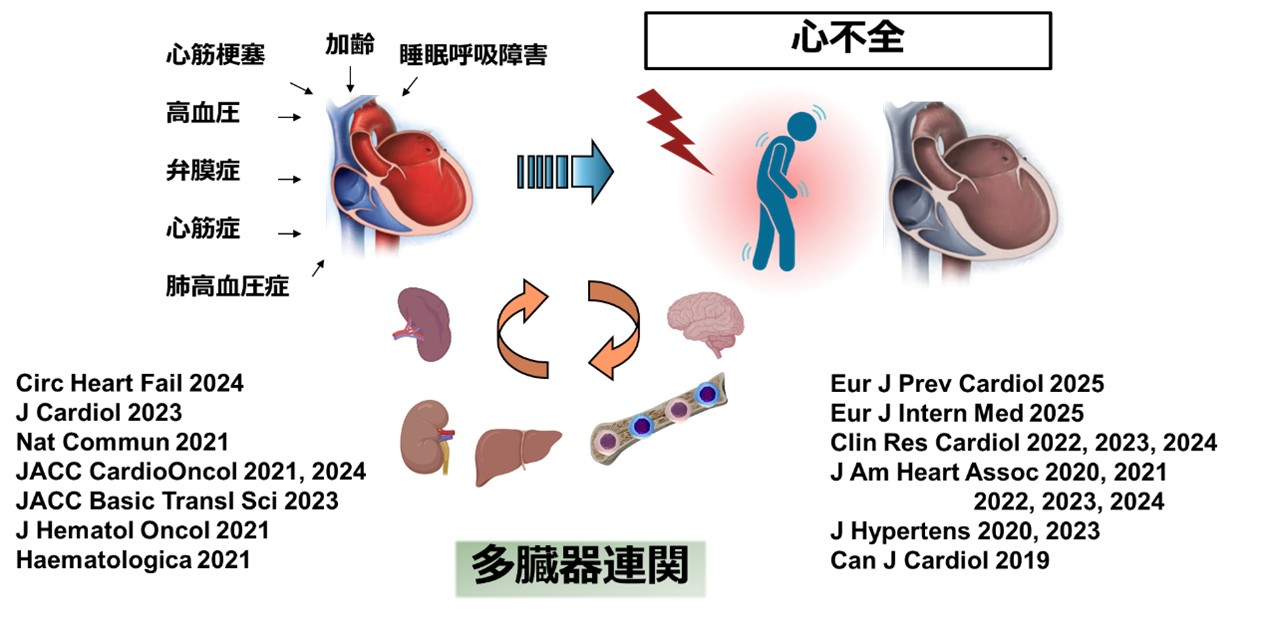
心不全は、複数の臓器が相互に影響し合いながら進展する疾患です。心不全を全身不全と捉えて、臓器間連関の分子基盤に基づき病態を解明することは、心不全克服に向けた重要なアプローチです。我々は、骨髄由来血球細胞の心不全に与える影響や、心臓・肝臓・腎臓・脾臓といった多臓器連関の病態メカニズムに注目し、研究を進めています。
好中球細胞外トラップと心不全
好中球は、自然免疫の中心的役割を担う白血球ですが、近年、好中球が放出する好中球細胞外トラップ (Neutrophil extracellular traps: NETs) が、炎症性疾患や血栓性疾患、がん、をはじめとする多様な病態と密接に関連することが明らかとなってきています。我々は、NETsが心不全の病態進展において重要な役割を果たすことを見出し、その分子機序の解明を進めてきました(Circ Heart Fail 2024; 17: e011057)。これらの成果から、NETsを標的とした治療が、心不全に対する新規治療ターゲットとなる可能性が示唆され、さらなる研究を進めています。
https://www.fmu.ac.jp/univ/kenkyuseika/research/20240607-2.html
https://www.fmu.ac.jp/univ/kenkyuseika/research/20240928.html
https://www.fmu.ac.jp/univ/kenkyuseika/research/230513.html
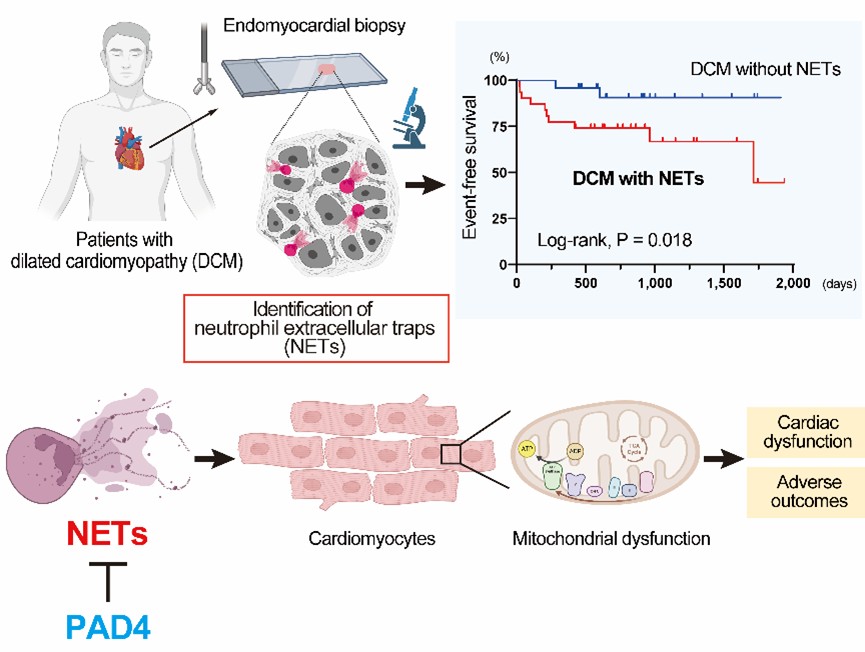
図. 心筋生検検体のNETsを同定することにより、NETsを有する心不全患者(拡張型心筋症患者)は予後不良と関連することが分かりました。マウス心不全モデルにおいて、ペプチジルアルギニンデイミナーゼ4(PAD4)の欠損によってNETsを抑制すると、心筋細胞のミトコンドリア機能は保持され、心機能の低下が抑制されることが明らかになりました。
クローン性造血と心血管疾患
クローン性造血とは、血液疾患のない健常な人でも、加齢とともに高い頻度で造血幹細胞に後天的な遺伝子変異が生じ、特定の血球クローンが増殖・拡大していく現象です。クローン性造血は、血液がんの前段階という従来の理解を超えて、心血管疾患をはじめとする多くの加齢関連疾患と深く関わっていることが明らかとなり、この10年間で研究が急速に進展してき分野です。我々は、輸血・移植免疫学講座と共同して、JAK2クローン性造血と心血管疾患における意義解明に取り組んでいます(Nat Commun 2021; 12: 6177、JACC CardioOncol 2021; 3: 134–136、Haematologica 2021; 106: 1910–1922、J Hematol Oncol 2021: 14: 52、J Cardiol 2023; 81: 3–9)。
https://www.fmu.ac.jp/univ/kenkyuseika/research/211026kimijima.html
https://www.fmu.ac.jp/univ/kenkyuseika/research/202012011.html
https://www.fmu.ac.jp/research/results/seika/2020/20200112.html
https://www.fmu.ac.jp/education/medicine/department/cardiovascular/research/research-f/PH.html
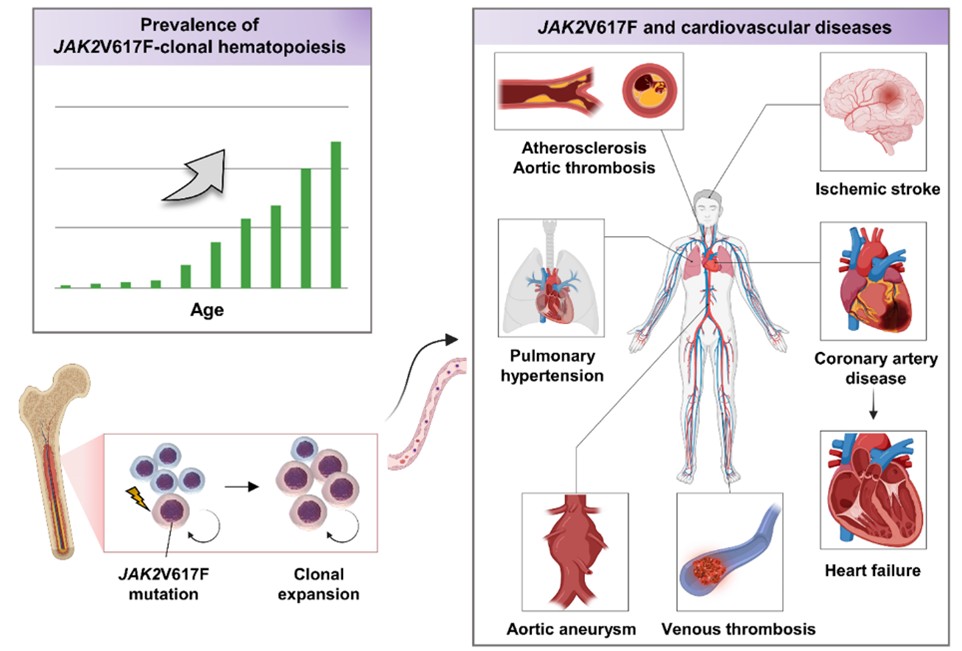
図. JAK2V617F変異により生じるクローン性造血は、加齢とともにその頻度が増加します。冠動脈疾患、心不全、肺高血圧症、静脈血栓症、大動脈瘤、虚血性脳卒中など、さまざまな心血管疾患と関連することが示唆されています。
心臓-肝臓連関におけるヘパトカインと心不全
肝臓から分泌されるホルモン・ヘパトカインは、全身の末梢組織に作用して、多様な生理機能を調節することから、心臓と肝臓の連関における新たな治療標的として注目されています。心不全患者において、肝臓から循環血中に分泌されるヘパトカイン・Fetuin-Aが低下し、Selenoprotein Pが上昇していることを見出してきました(Clin Res Cardiol 2022: 111: 1104-1112. J Am Heart Assoc 2022; 11: e024901、J Am Heart Assoc 2024; 13: e035139)。これらの変化は、心不全の予後不良と関連していることから、心臓-肝臓連関におけるヘパトカインが、心不全病態における重要な役割を果たすことが示唆され、さらなる研究を進めています。
https://www.fmu.ac.jp/univ/kenkyuseika/research/220610.html
心臓-脾臓連関と心不全
脾臓は、免疫の司令塔のひとつとして重要な役割を担っています。末梢血における単球/マクロファージ関連分子であるCD36 mRNA発現の増加が、脾臓の構造的リモデリングと関連する可能性が示唆され、心不全における慢性炎症状態と、脾臓を介した免疫細胞の動員や再構築が、病態進展に関与して可能性が示唆されます(Clin Res Cardiol 2023; 112: 942–953)。
https://www.fmu.ac.jp/research/results/seika/2023/230420-2.html
2. 心筋細胞の恒常性を支える分子機構
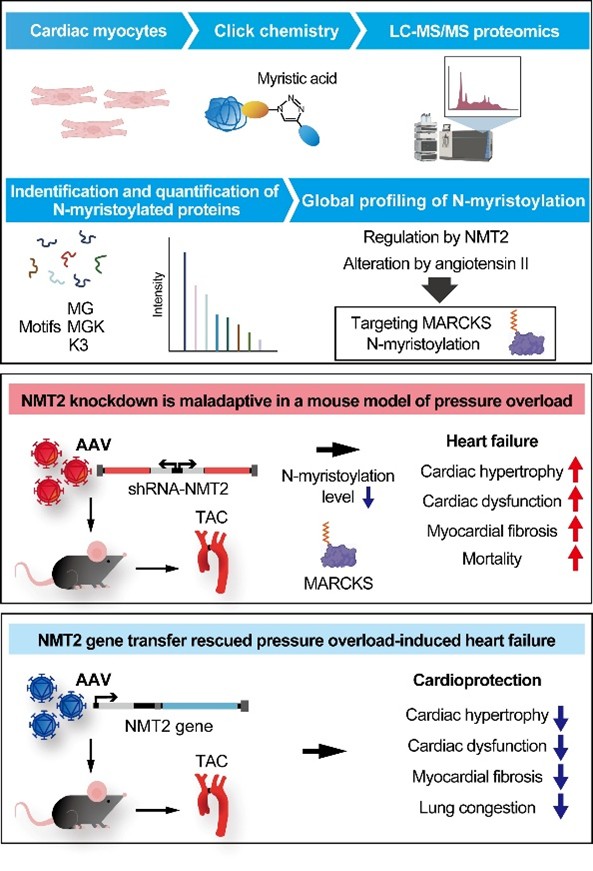
心筋細胞の恒常性維持機構とそれを取り巻く多様な細胞・分子群を、「心臓微小環境」ととらえています。成人の心筋細胞はほとんど分裂しないため、心筋細胞の恒常性を支える分子基盤は重要な役割を果たしております。我々は、Nミリストイル化という蛋白質翻訳後修飾の心不全における意義を明らかにしてきました(JACC Basic Transl Sci 2023: 8: 1263-1282)。クリックケミストリーと定量的プロテオミクスを応用したアプローチにより、心筋細胞において、心不全病態における重要なN-ミリストイル化蛋白質を同定しました。アデノ随伴ウイルス9を介した心臓特異的なN-ミリストイル転移酵素の遺伝子導入により、圧負荷モデルマウスにおける心機能障害が抑制出来ることを示しました(図)。
https://www.fmu.ac.jp/univ/kenkyuseika/research/20231018.html
https://www.fmu.ac.jp/univ/kenkyuseika/research/230126_2.html
https://www.fmu.ac.jp/research/results/hyosyo/2022/230126_2.html
3. 心不全におけるミトコンドリア
心臓は、休むことなく拍動し続けるために、心筋細胞内には多数のミトコンドリアが存在し、その機能維持は心機能の恒常性を保つために不可欠です。細胞胞骨格構造の一種であるα-チューブリンの脱チロシン化が、心不全におけるミトコンドリア機能障害およびオートファジーの抑制に深く関与していることを明らかにしました。脱チロシン化α-チューブリンは、ミトコンドリア表面に異常に集積し、ParkinのリクルートやVDAC1のユビキチン化を妨げることで、ミトコンドリア機能異常につながる分子機序を解明しました(FEBS Lett 2025; 599: 2474-2490)。
4. エピジェネティクスと心不全
心不全は、その多くが遺伝的因子と環境的因子が影響する多因子疾患です。環境的因子として注目されているのが、エピジェネティクスとよばれるDNAの塩基配列変化によらない遺伝子発現を制御する機構です。エピジェネティクスには、ヒストン修飾とDNAメチル化が含まれ、クロマチンの構造的変化をさせることなどによって、DNAの転写調節に関与します。私たちはこれまでに、心不全患者における血液細胞のDNAメチル化変化に着目し、炎症関連分子FKBP5遺伝子の低メチル化が心不全と関連することを明らかにしてきました(J Am Heart Assoc 2021; 10: e021101)。さらに現在、新規ヒストン修飾に着目した研究も進めており、エピジェネティックな制御機構を遺伝的背景によらない修飾可能な治療ターゲットとして応用する可能性を探っています。
https://www.fmu.ac.jp/univ/kenkyuseika/research/20250514.html
https://www.fmu.ac.jp/research/results/hyosyo/2025/20250514_2.html
https://www.fmu.ac.jp/research/results/hyosyo/2025/20250514_8.html
5. 心不全と臓器連関における細胞外小胞(エクソソーム)
細胞外小胞は、細胞が分泌する膜で包まれた微小な粒子であり、細胞間コミュニケーションを担う重要な分子輸送体として注目されています。エクソソームは、直径30〜150 nm程度の最も小型の細胞外小胞で、エンドソーム由来の膜構造をもち、さまざまな生理・病理学的過程に関与しています。現在、我々は心不全の臓器連関において、エクソソームが果たす役割とその分子メカニズムの解明に取り組んでいます。
6. 心不全とがん進展におけるNGF–TRAKの役割
近年、慢性心不全患者ではがん発生率が増加することや、心筋梗塞後の心不全患者は、がんの発症率が高いことが報告されています。我々は、そのメカニズムを解明するために、マウスモデルを用いて研究を行い、神経成長因子(NGF)とその受容体TrkAの活性化が、がんの進展に関与していることを明らかにしました(JACC CardioOncol 2024; 6: 55-66)。
このことは、心不全とがんとの病態連関を示す重要な知見となっています。
https://www.fmu.ac.jp/research/results/hyosyo/2022/221128.html
文責:三阪智史

