心臓電気生理・不整脈疾患
近年、不整脈疾患に対する治療デバイスは目覚ましく進歩しており、より効果的で低侵襲な治療が可能となっています。頻脈性不整脈に関しては、従来は高周波カテーテルアブレーションが主な治療法でしたが、現在は様々なエネルギー源(クライオアブレーション、パルスフィールドアブレーション等)が選択可能となっています。不整脈機序を解明するためのナビゲーションシステムも進歩しており、各種画像モダリティ(心エコー、CT、MRI等)と組み合わせることで、より高精度な治療が可能となっています。
また、ペースメーカーをはじめとしたCIED(植込み型心臓電気デバイス)の進歩により、体への侵襲度をより小さく、かつ多機能なCIEDが臨床応用されており、徐脈性不整脈のみならず、心不全治療においても重要な役割を果たしています。
当科では、最先端の治療デバイスを用い、患者さんの予後やQOL(生活の質)の向上を目指した診療を行っています。
カテーテルアブレーション
主に足の付け根にある血管(動脈や静脈)からカテーテルを心臓内に挿入し、ナビゲーションシステムを用いることで心臓内の不整脈のメカニズムを解析・可視化します。この解析結果をもとに、各種治療カテーテルを用いて不整脈を抑制します。当科では1994年のカテーテルアブレーション導入以降、約3000例の症例に対して施行しており、実施症例数は年々増加しています。(グラフ1)
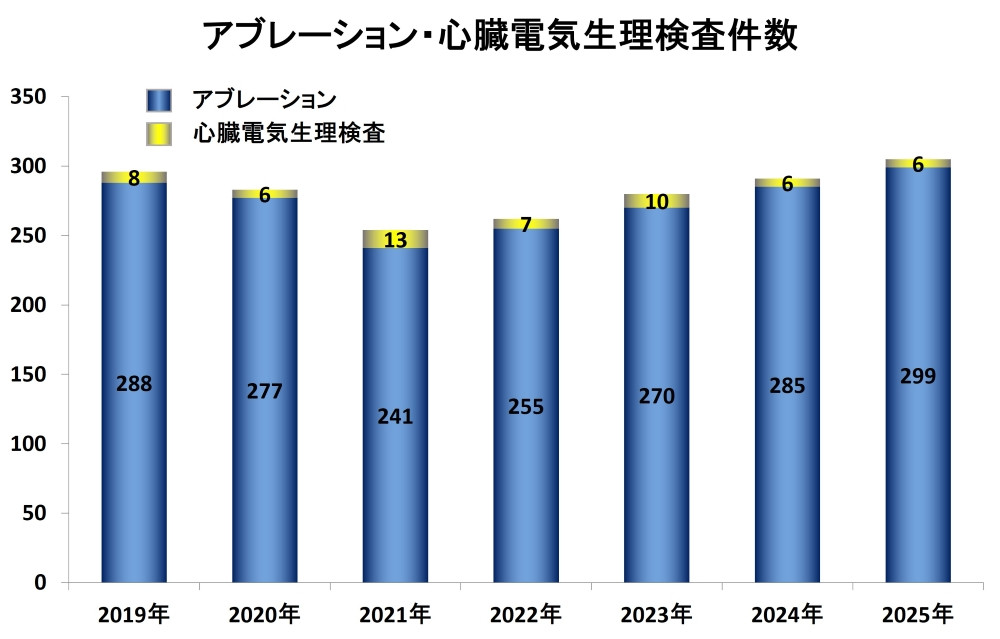
グラフ1
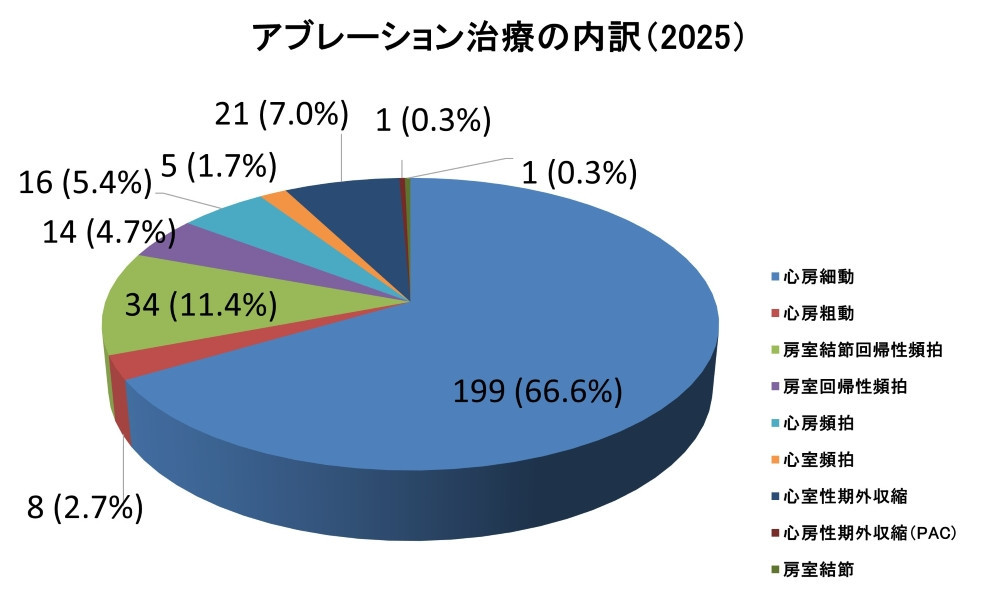
カテーテルアブレーションは、すべての頻脈性不整脈に対して適応があります。グラフ2に、当科における直近2025年のカテーテルアブレーション治療内訳を示します。症例数が最も多いのは心房細動であり、全体の約7割を占めています。これは全国的にも同様の傾向です。
心房細動に対するカテーテルアブレーション
心房細動は、左心房に接続する左右2本ずつ、計4本の肺静脈を起源として生じます。カテーテルアブレーションにより左心房と肺静脈との電気的な接続を遮断することで心房細動を抑制します。この治療法は「肺静脈隔離術」と呼ばれ、心房細動に対するカテーテルアブレーションの標準治療です。
かつては高周波カテーテルアブレーションのみが用いられていましたが、その後クライオバルーンアブレーションが導入され、2024年からはパルスフィールドアブレーションも使用可能となりました。パルスフィールドアブレーションは、カテーテルから非常に高い電圧を超短時間心臓に送出することで、熱を用いずに治療対象となる心筋細胞を選択的に障害する治療法です。そのため手術時間が短く(60~90分)、合併症リスクも大幅に低減できることから急速に普及しており、当院でも多くの症例で本治療を行っています。(図1)

図1
CIED(植込み型心臓電気デバイス)植込み
徐脈性不整脈(洞不全症候群、房室ブロック)に対して、ペースメーカー植込み術を行っています。現在、多くのペースメーカーはMRI対応型であり、一定の条件を満たせば術後もMRI検査が可能です。
リードレスペースメーカー
従来の経静脈リードを用いたペースメーカーでは、制御回路と電池を内蔵したジェネレーターを前胸部皮下に植え込み、心臓内に留置したリードを介して電気刺激を行っていました。これに対しリードレスペースメーカーは、直径6mm、全長18mmのジェネレーターを内蔵した本体に電極を直接備え、機器全体の小型化を実現しています。本体を直接右心室内に留置することで、皮下ポケット形成およびリードを不要としました。
長所
1. ポケット作成に伴う創部感染リスクを回避できる。
2. リード留置に伴う血管損傷、リード感染、リード断線などのリードトラブル(2.4~5.5%)を回避できる。
3. 鼠径部からのカテーテル操作のみで留置が可能なため、手術時間の短縮が期待できる。
短所
1. シングルチャンバーペースメーカーであり、心室のみをペーシングするVVI機能に限定される。
2. 電池寿命到達時に本体の抜去が困難な場合が多く、必要に応じて右心室内に追加留置が必要となる。
これらの長所・短所を踏まえ、患者さんの状態に応じて通常型ペースメーカーまたはリードレスペースメーカーの適応を判断しています。

リードレスペースメーカー
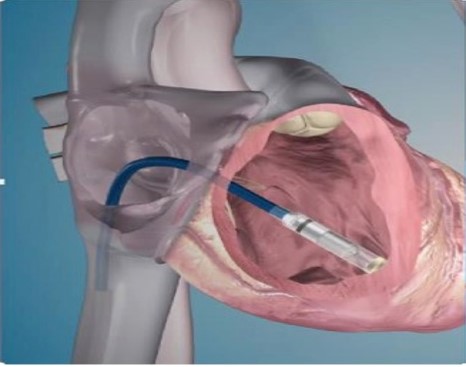
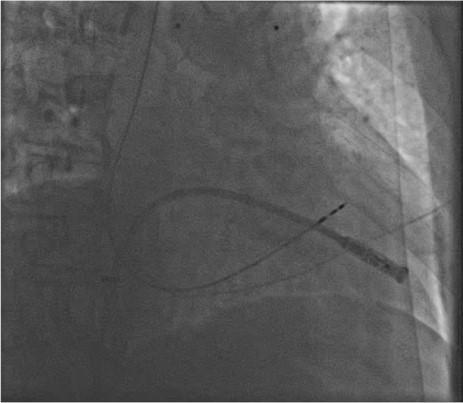
右心室心尖部への留置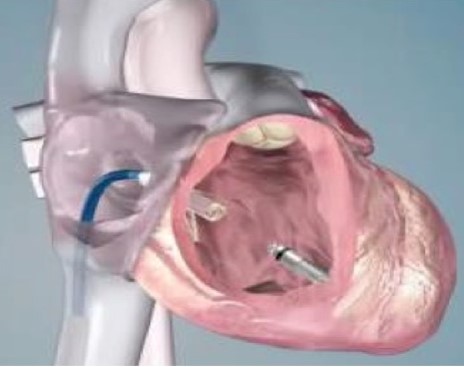
本体の分離及びカテーテル抜去
植込み型除細動器(ICD)
日本では年間約5万人が心臓突然死を来すと推定されており、その主な原因は心室細動です。心室細動では心臓が有効に拍動できず、数秒で失神し、数分で生命に関わる状態となります。これを救命する唯一の有効な方法が電気ショックによる除細動です。この除細動器を小型化し、体内に植え込む形としたものが植込み型除細動器(ICD)です。
従来は心臓内にショックリードを留置する経静脈ICDが主流でしたが、現在では全システムを皮下に留置する皮下植込み型ICD(S-ICD)も使用可能となっています。
S-ICDの長所
1. 心臓・血管内にリードを留置しないため、リード関連合併症を回避できる。
2. 本体・リードとも皮下にあるため、感染時も全身感染に進展しにくく、抜去が可能である。
S-ICDの短所
1. 徐脈性不整脈に対するペーシング機能を有しない。
2. 抗頻拍ペーシングが行えないため、適応が限定される。
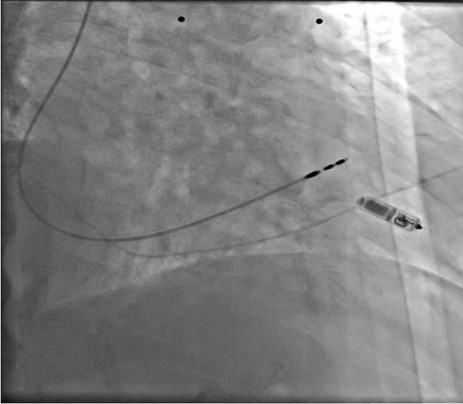
皮下植込み型除細動器
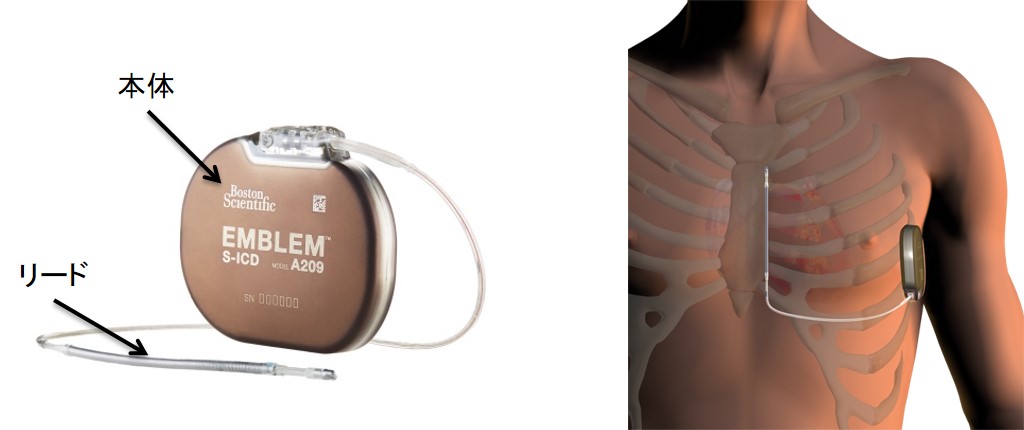
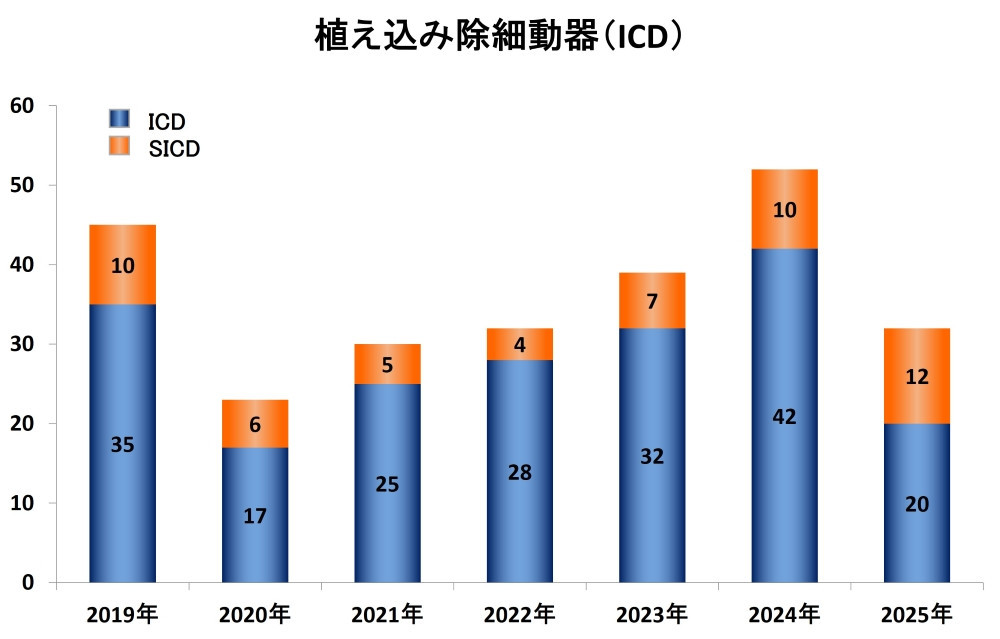
当科におけるICD植え込み数の推移
心不全に対する心臓再同期療法(CRT)
心不全では心室内の興奮伝導にずれが生じ、心臓の収縮効率が低下します。右心室と左心室を同時にペーシングすることで収縮の同期性を改善し、心機能や併存する弁膜症の改善を図る治療が心臓再同期療法(CRT)です。当院は植込み認定施設であり、専門講習を受けた認定医が治療を担当しています。
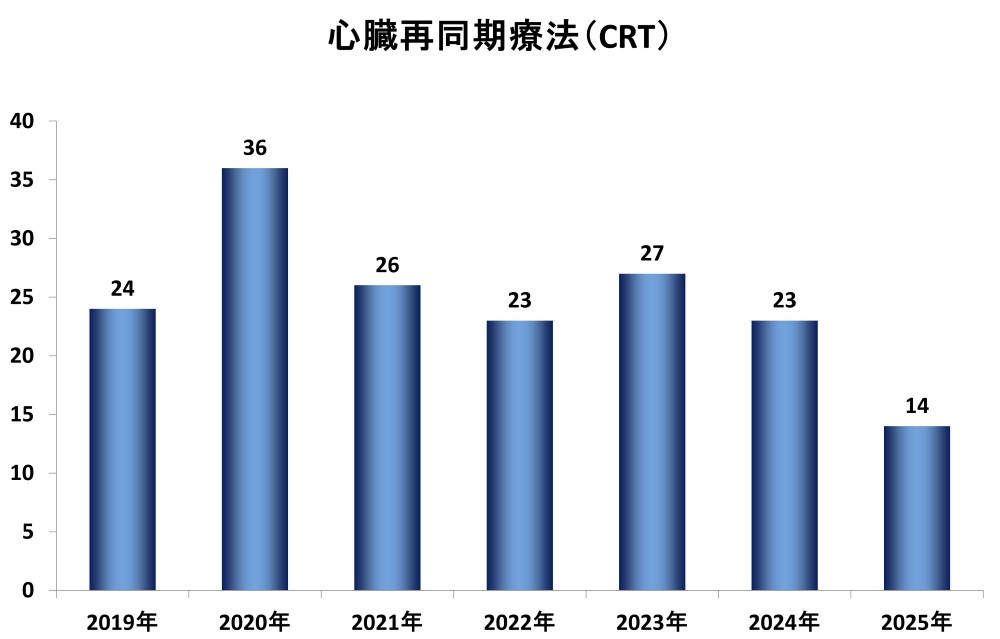
当科におけるCRT植え込み数の推移
CRTにより僧帽弁逆流が改善した一例の胸部X線と心エコー図
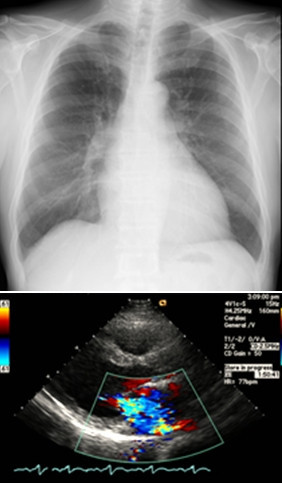
入院時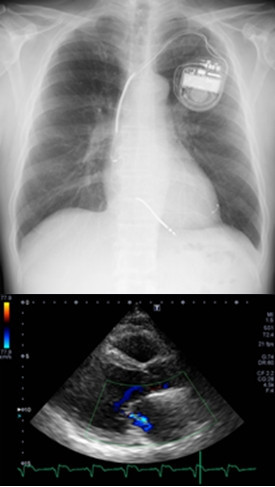
CRT-D植え込み後
右室ペーシングからCRT-Dにup-gradeした前後の胸部X線写真
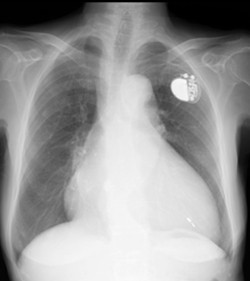
入院時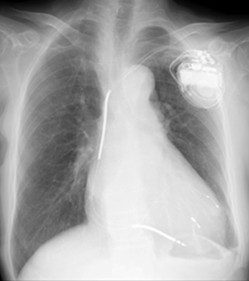
CRT-D植え込み後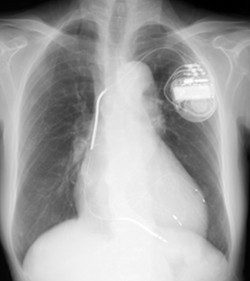
植え込み半年後
遠隔モニタリング
ICDなどのCIEDに内蔵された通信機能を用い、インターネットを介してデバイス作動状況や患者さんの状態を把握する遠隔モニタリングを導入しています。不整脈や心不全の早期対応、デバイス不具合の管理を、医師・臨床工学技士・看護師が連携して行っています。
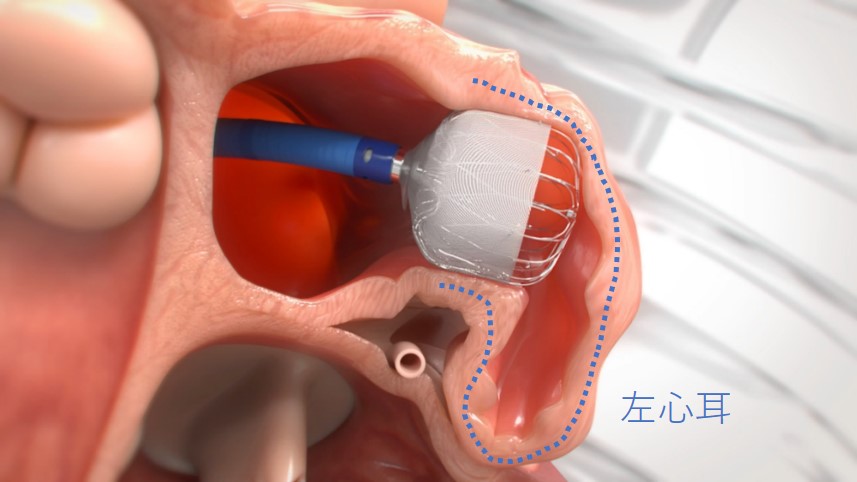
経皮的左心耳閉鎖術
心房細動による心原性脳塞栓症予防には抗凝固療法が重要ですが、出血リスクが高く継続が困難な患者さんも存在します。経皮的左心耳閉鎖術は、塞栓源となる左心耳を閉鎖することで脳塞栓症を予防する治療法で、わが国では2019年より保険適用となっています。各種臨床試験により、その安全性と有効性が示されています。
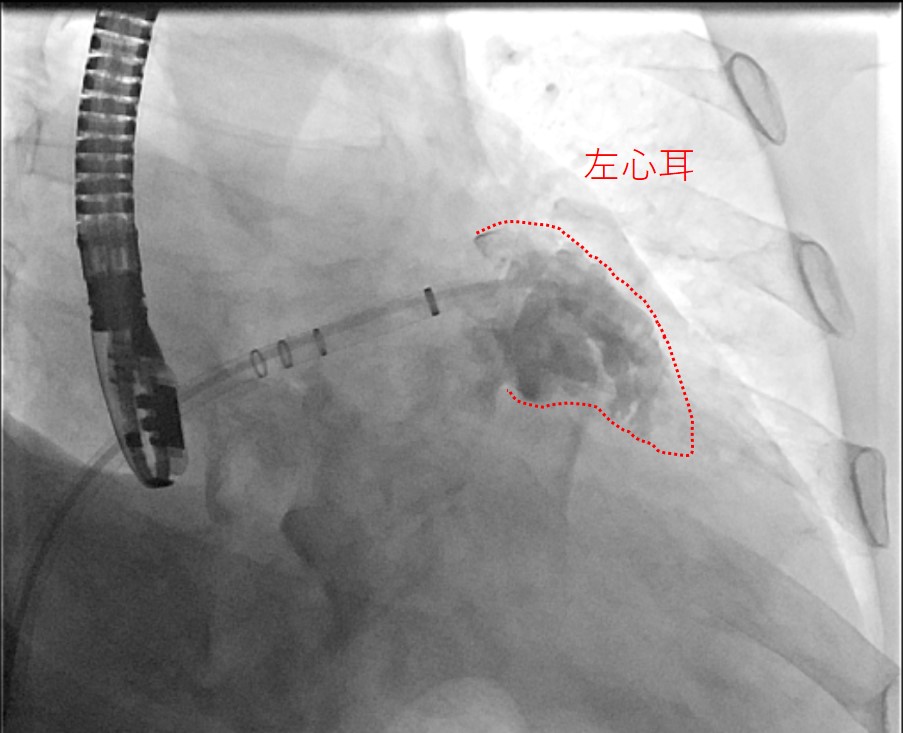
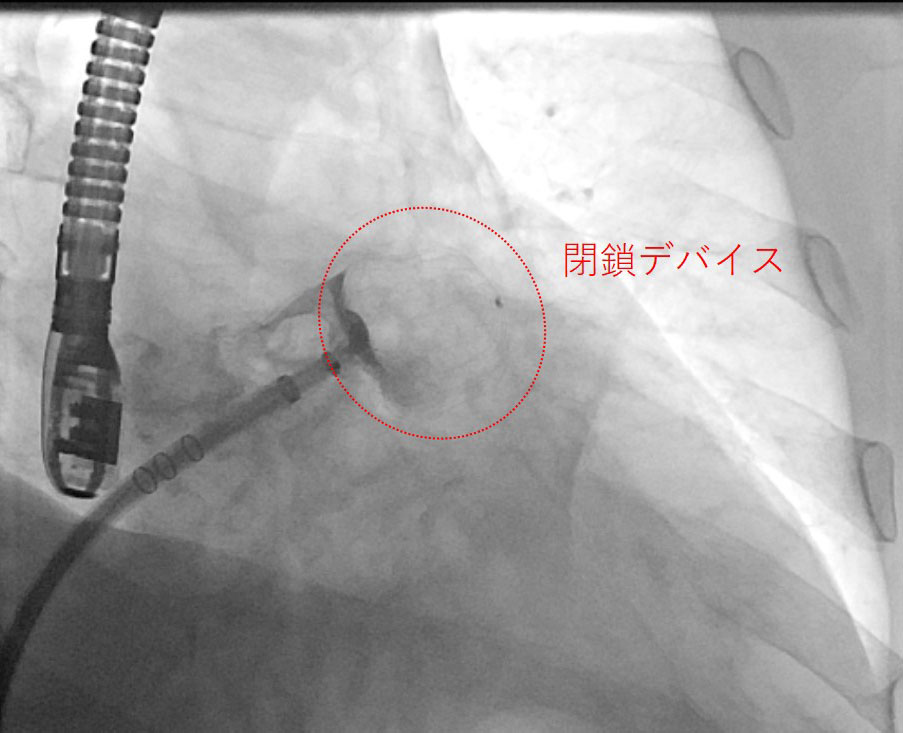
術中透視画像
術中経食道心エコー
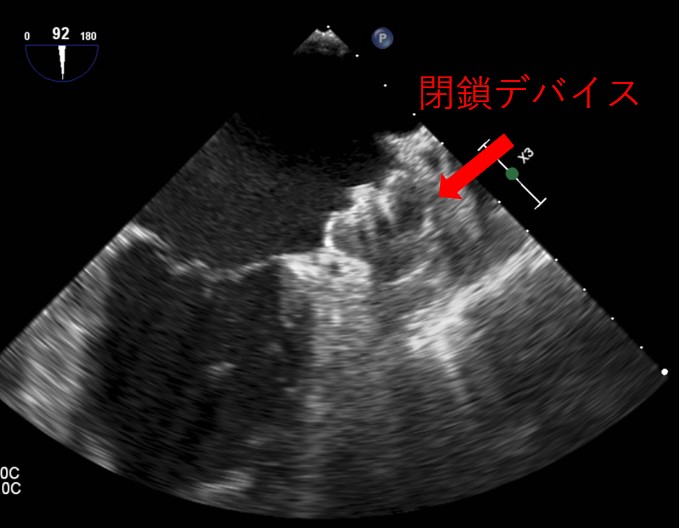
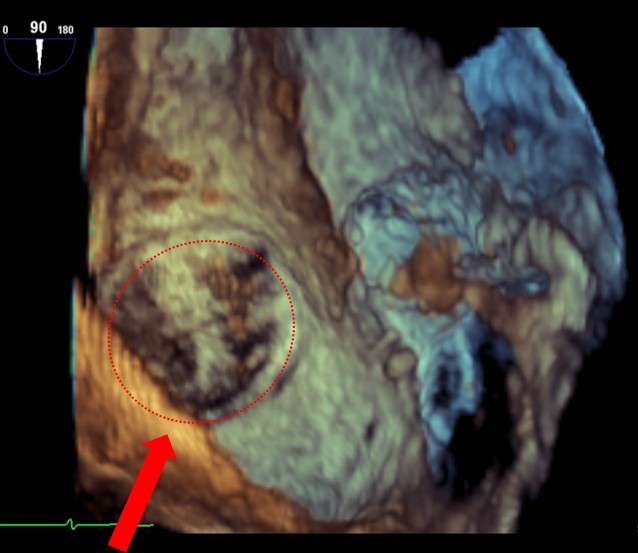
左心耳入口部(心腔内より)
留置前 3D画像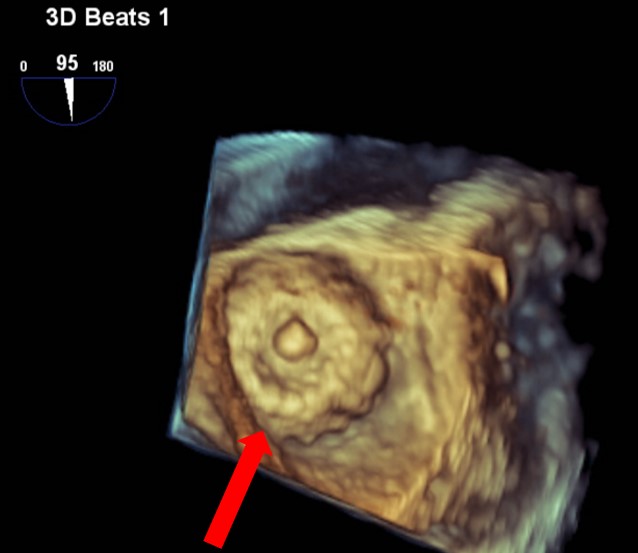
デバイスで閉鎖された左心耳
留置後 3D画像
文責:金城貴士