
- 杉本 幸太郎(すぎもと・こうたろう)
- 医学部 基礎病理学講座 講師

- 小島 学(こじま・まなぶ)
- 医学部 基礎病理学講座 博士研究員
- 研究グループ
- 基礎病理学講座 杉本幸太郎、小島学、千葉英樹
産婦人科学講座 藤森敬也
概要
論文掲載雑誌:「Molecular Cancer Research 」(2021年3月16日)
我々は以前、細胞間接着分子クローディン-6からエストロゲン受容体に至る新しいシグナル伝達経路を発見しました(Sugimoto et al., PNAS, 2019)。エストロゲンは女性ホルモンの1種で、エストロゲン受容体に結合することで細胞の遺伝子発現を調節します。子宮体がんではエストロゲンやエストロゲン受容体がその発生と進展に寄与することが古くから知られていました。そこで前述のシグナル経路が子宮体がんの悪性化にはたらくのではないかと仮説を立てて研究を進めました。
まずクローディン-6のタンパク質発現を定量的に測ることができる病理診断用の抗体を独自に開発しました。続いて福島県立医大およびいわき市医療センターにおける子宮体がん患者の手術検体(病理標本)を集め、そのクローディン-6発現を評価して生存期間などとの関連を評価しました。その結果、クローディン-6が発現していない、もしくは少量しか発現していない患者では5年後の生存率が約90%と高いのに対し、クローディン-6が高発現している患者では5年後の生存率が約30%まで低下しており、クローディン-6が子宮体がんの有望な予後予測マーカーであることがわかりました(第一論文)。具体的な展望として、子宮体がんの病理検査の際に従来の進行度(ステージ)などに加えてクローディン-6の発現量を評価し、低発現なら再発の可能性が低いので経過観察のみ、高発現なら術後化学療法を追加して再発を防ぐといった応用が考えられます。
(第一論文掲載ページ:http://www.fmu.ac.jp/univ/kenkyuseika/research/20201013.html )
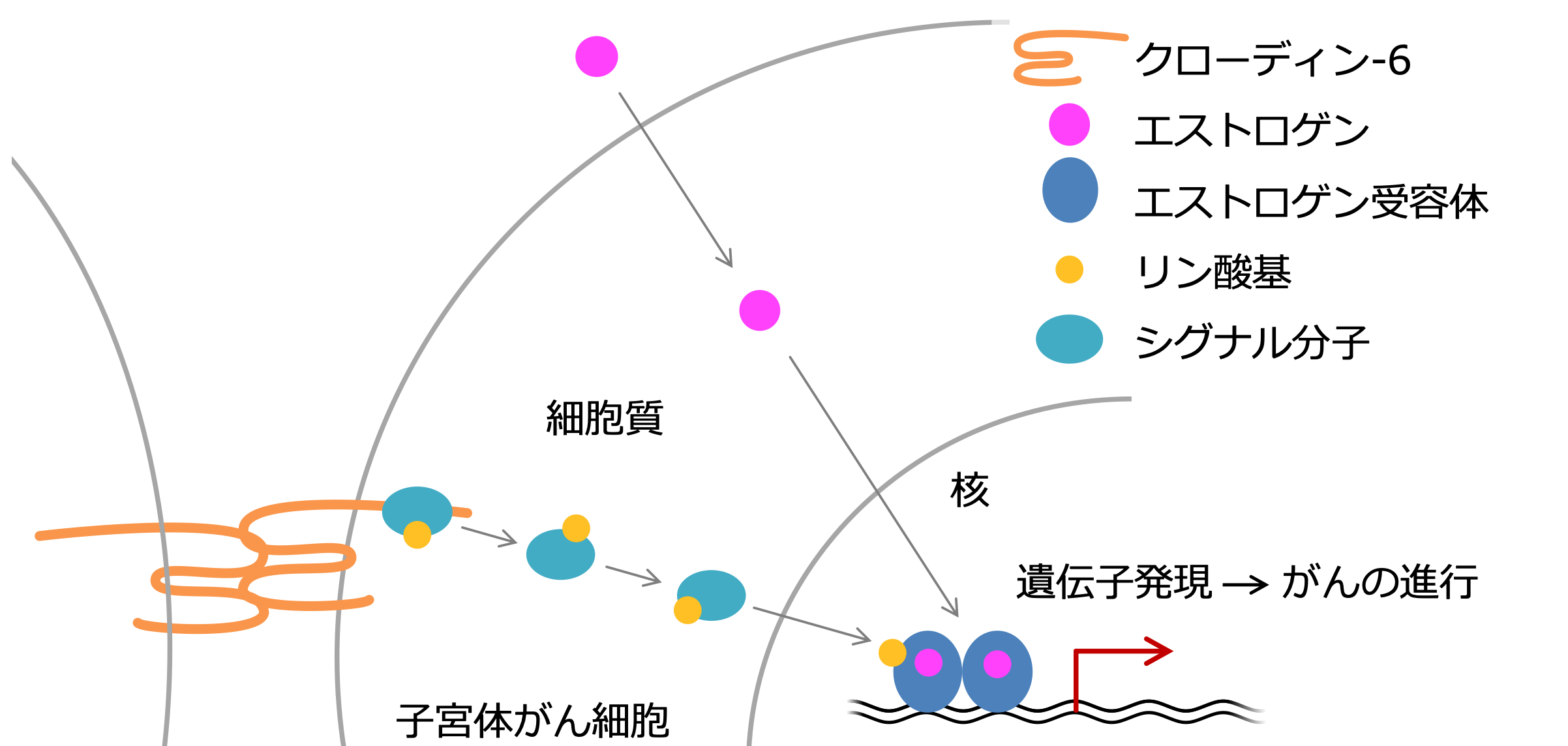
続いてクローディン-6による悪性化のメカニズムを探るため、子宮体がん細胞株を用いて分子生物学的に検討しました。その結果、クローディン-6による細胞間接着シグナルがエストロゲン受容体を異常にリン酸化して活性化させ、活性化したエストロゲン受容体ががん関連遺伝子の発現を変化させることによって、細胞の増殖や転移の元となる細胞遊走能を亢進することがわかりました。またクローディン-6によるエストロゲン受容体活性化は、エストロゲンに対するエストロゲン受容体の感受性を高め、通常なら反応しないごく少量のエストロゲンでも受容体が活性化してしまうためであることが示されました(第二論文)。
これまで子宮体がんの治療では、エストロゲン受容体を抑制するためにエストロゲンを阻害するアプローチがなされてきましたが、それが効かない症例や治療中に耐性が出現する症例も多いことが問題でした。本研究によりエストロゲン受容体に対する薬物療法として、従来のエストロゲンそのものだけでなく、クローディン-6やクローディン-6とエストロゲン受容体の間のシグナル分子群、あるいはエストロゲン受容体のリン酸化部位が新規治療標的となる可能性が示されました。
これら一連の研究は、子宮体がんにおいてクローディン-6が予後予測マーカーおよび治療標的となることを明らかにし、同がんの個別化治療戦略の発展に寄与するものです。
連絡先
公立大学法人福島県立医科大学 医学部基礎病理学講座
電話: 024-547-1169
講座ホームページ:https://www.fmu.ac.jp/home/p2/index.html
メールアドレス:sugikota@fmu.ac.jp(スパムメール防止のため、一部全角表記しています)

