
- 髙住 美香(たかすみ・みか)
- 医学部 免疫学講座 大学院生

- 石田 由美(いしだ・ゆみ)
- 医学部 免疫学講座 専門医療技師

- 町田 豪(まちだ・たけし)
- 医学部 免疫学講座 講師

- 関根 英治(せきね・ひではる)
- 医学部 免疫学講座 教授
- 研究グループ
- 髙住美香1,2、大森智子1、町田豪1、石田由美1、林学1,2、鈴木俊幸3、本間好4、遠藤雄一1、高橋実1、大平弘正2、藤田禎三5、関根英治1
1: 福島県立医科大学・免疫学講座
2: 福島県立医科大学・消化器内科学講座
3: 福島県立医科大学・放射性同位元素研究施設
4: 福島県立医科大学・生体物質研究部門
5: 福島県立総合衛生学院
概要
論文掲載雑誌:「FASEB Journal」(2020年3月オンライン)
公立大学法人福島県立医科大学 医学部 免疫学講座 髙住美香大学院生(現消化器内科学講座助教)、石田由美専門医療技師、町田豪講師、関根英治教授らは、自然免疫機構の1つである「補体系」の活性化を阻害する融合タンパク質「sMAP-FH」を新たに開発しました。抗補体薬として、炎症性疾患に対する新規治療薬として用いられることが期待されます。
約30種類のタンパク質で構成される補体系は、古典経路・レクチン経路・第二経路という3つの異なる経路を通じて活性化されます。その結果、補体タンパク質C3は活性化し、病原微生物やアポトーシスを起こした細胞に結合して「異物」としてこれらを標識し、食細胞による異物の貪食処理を促します。さらに反応が進むと、補体系は異物を直接破壊することもできます。しかし、補体系の過剰、もしくは無秩序な活性化は炎症を増悪し、さまざまな臓器障害を引き起こします。
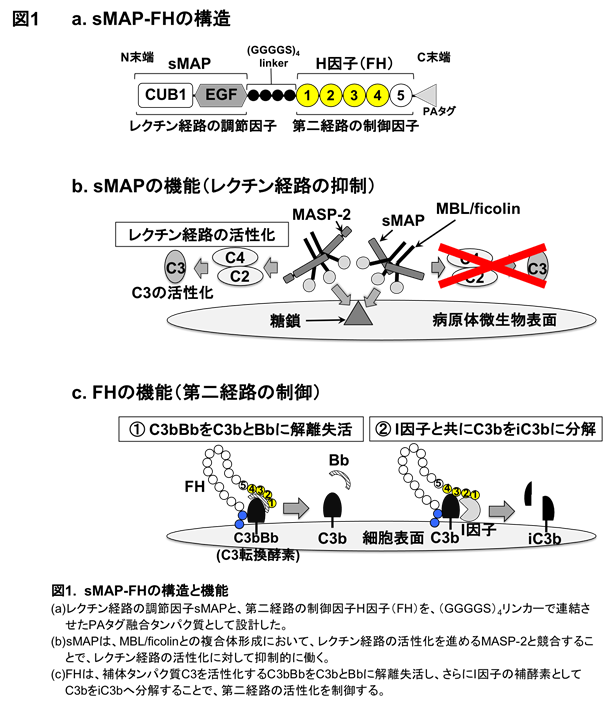
今回我々は、レクチン経路と第二経路の活性化を阻害する治療薬の開発を目的に、レクチン経路の活性化を調節する生体内の補体因子「sMAP」と、第二経路の活性化を制御する生体内の「H因子(FH)」の一部を、分子生物学的手法で連結させた融合タンパク質「sMAP-FH」を作成しました(図1a)。
sMAPは、レクチン経路の活性化を進めるセリンプロテアーゼMASP-2のスプライシングバリアント*です。生体内において、sMAPとMASP-2は両者の共通構造を介してレクチン経路の認識分子であるMBL/ficolinと複合体を形成しています。その複合体が病原微生物表面の糖鎖を認識するとMASP-2が活性化され、レクチン経路の活性化が進みます。一方、酵素活性を持たないsMAPは、MBL/ficolinへの複合体の形成をMASP-2と競合することで、レクチン経路の活性化に抑制的に働くことが示されています(図1b)。
一方H因子は、C3を活性化する第二経路のC3転換酵素C3bBbをC3bとBbに解離失活し、さらにI因子の補酵素としてC3bをiC3bへ分解することで第二経路の活性化を抑制する因子です(図1c)。
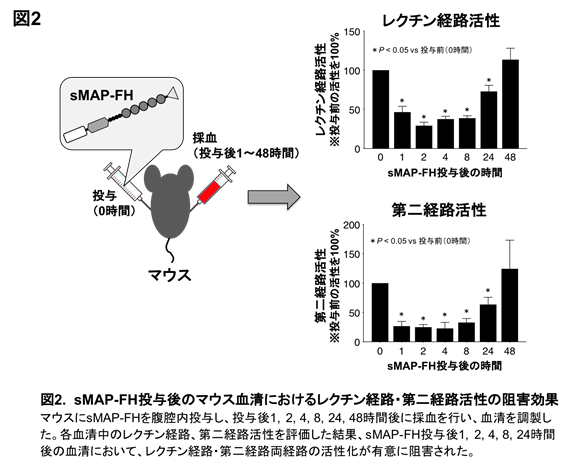
今回、マウス型のsMAP-FHをマウスに投与し、採取した血清を解析した結果、レクチン経路と第二経路の活性化の有意な阻害効果を認めました(図2)。さらにヒト型のsMAP-FHを開発し、ヒト血清への添加によるレクチン経路と第二経路の活性化の阻害効果も確認しました。
近年、加齢黄斑変性、臓器の虚血再灌流障害、炎症性腸疾患など、多くの炎症性疾患でレクチン経路と第二経路の活性化が、炎症を惹起することや増悪を増悪することが示されています。本研究により、抗補体薬「sMAP-FH」がそれらの炎症性疾患に対する新たな治療薬として用いられることが期待されます。
スプライシングバリアント*:1つの遺伝子から作られ、構造や機能が異なる複数のタンパク質(変異体)をいう。
連絡先
公立大学法人福島県立医科大学 医学部 免疫学講座
電話:024-547-1148
FAX:024-548-6760
メールアドレス:immunol@fmu.ac.jp(スパムメール防止のため、一部全角標記しています)

