研究テーマ
|
|
1. PET/MRIを用いた心疾患の病態評価に関する研究
2. 3D-OSEM法を用いたSPECT再構成法に関する検討 |
心臓核医学の分野では、主にPET/MRIを用いた心臓イメージングの研究を行っています。PET/MRIは2013年に当院へ設置され、臨床・研究に利用されてきました。当科でも様々な疾患に対してその病態解明や臨床応用の研究を行っています。
現在、当院で合成可能な18F-fluorodeoxyglucose (FDG)、13N-ammoniaを用いた様々な研究を行っていますが、新規薬剤を用いた新しい臨床研究を今後計画しています。
従来の心筋血流SPECTに関しても、新しい再構成法などを用いて、診断能向上に向けて研究を行っています。
|
18F-FDG PET/MRIを用いた心筋バイアビリティの研究
|
18F-fluorodeoxyglucose (FDG)はブドウ糖を18-フッ素で標識した放射性薬剤です。一般的には悪性腫瘍の病態評価に多く用いられていますが、心臓にも応用することができます。
心臓の代謝はブドウ糖・脂肪酸の両方で行われており、FDG PETにより心臓の糖代謝を評価することができます。普段は心臓の代謝は脂肪酸が優位ですが、食事の影響などでブドウ糖と脂肪酸の使われる比率が変わります。また、病的な状態では心筋虚血などの影響で代謝は脂肪酸からブドウ糖にシフトします。長時間の虚血にさらされた心筋は収縮能の低下を起こし、虚血が解除されると徐々に心機能が改善します。そういった心筋は冬眠心筋
(ハイバネーション)と言われており、生きている (バイアビリティのある)心筋として、死んでしまった心筋とは区別されます。心エコーなどの心臓の形態だけの評価では、死んで瘢痕化してしまった心筋なのか、ハイバネーションなのかを区別することができません。ハイバネーションの状態では最低限のブドウ糖代謝が行われており、FDG
PETではそれを区別する事が可能です。
一方で、心臓MRIも現在は心筋バイアビリティの評価に用いられています。心臓MRIではガドリニウム造影剤の遅延造影を用いて、心筋の線維化を描出することが可能です。これは、ブドウ糖代謝と違い、死んで線維化してしまった心筋を描出することが可能で、PETにより得られる画像と反対の情報となります。
PET/MRIを用いることで、PETによるブドウ糖代謝とMRIによる心筋の線維化の評価を同時に行うことが可能となります。両者は裏表の関係にあることが予想されますが、これまで両者の関係は十分に検討されておらず、この研究で心筋バイアビリティの病態をより深く評価することが可能と考えています。現在、慢性虚血性心疾患の患者を対象として、従来のPETあるいはMRIのいずれかだけではなく、PET/MRIにより両者を同時に評価してその関連を研究しています(図1)。
|
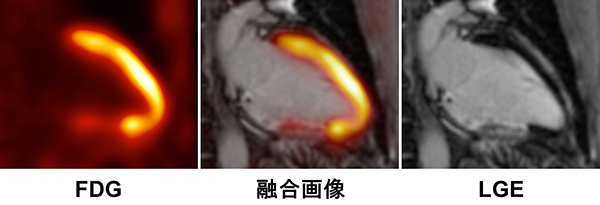 |
図1
下壁の心筋梗塞の症例です。ガドリニウム遅延造影像で下壁に造影の陽性領域を認め、FDGではそれに一致してFDGの集積の高度低下を認めます。
|
18F-FDG PET/MRIを用いた心臓サルコイドーシスの研究
|
18F-FDGはブドウ糖代謝だけでなく活動性炎症にも集積することがわかっています。炎症性の心疾患である心臓サルコイドーシスは、PETによる診断が有用な疾患です。心臓サルコイドーシスは、発症すると致死性の不整脈や心不全を起こすため、早期発見・早期介入が重要です。これまでの検査では、心臓の形態や運動を評価することができても、活動性の炎症を評価することができませんでした。また、ガリウムシンチグラフィでは活動性の炎症を評価することが可能ですが、検査感度が低いため偽陰性の結果になることが多い検査です。
PETは心臓サルコイドーシスの診断において感度が高く、病変の検出に非常に優れた検査です。さらに、MRIでは心臓の形態や壁運動だけでなく、心筋の浮腫や線維化といった性状も評価可能です。PET/MRIを用いることでその両者を1度の検査で評価可能であり、心臓サルコイドーシスの様々な病態の評価を行うことができます。我々はPET/MRIを用いて心臓サルコイドーシスを評価することで、PET/MRIの診断への有用性だけでなく、PETとMRIの所見の違いを含め検討を行っています(図2;
文献5を改変して掲載)。
|
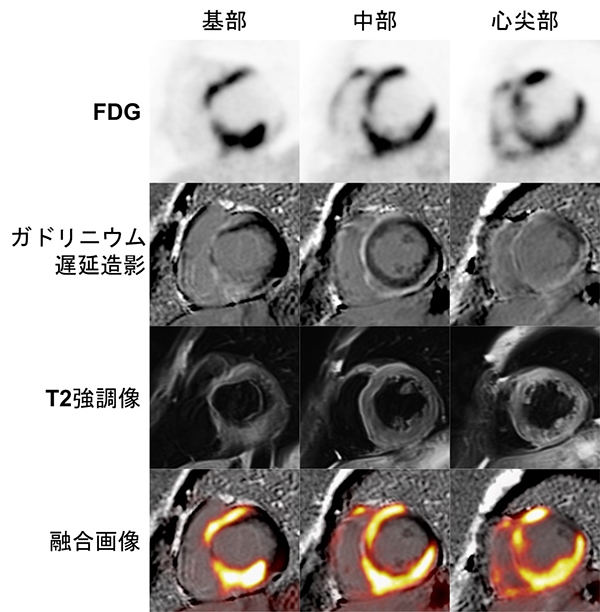 |
図2
心臓サルコイドーシスの症例です。FDGの集積に一致するようにガドリニウム遅延造影での陽性像、T2強調像を認めますが、いずれも陽性領域が異なっており、それぞれのモダリティで異なった病態を評価していることがわかります。
|
18F-FDG PET/MRIを用いた動脈プラークの研究
|
18F-FDGの活動性炎症に集積する特徴を用いて、動脈プラークの研究を行っています。不安定プラークはその形成に炎症が関与しており、FDG PETで検出が可能です。我々は現在、腸骨動脈領域の動脈プラークの検討を行っています。プラークの性状評価として、FDG
PETによる炎症の評価、MRIによる組織性状の評価、血管内超音波 (IVUS)による侵襲的な評価を加え、プラークの性状とFDG集積との関連を研究しています(図3;
文献4を改変して掲載)。最終的には冠動脈や大動脈の動脈プラークを評価することで、心血管イベントの予後予測や治療適応の決定に役立てる研究を行う予定です。
|
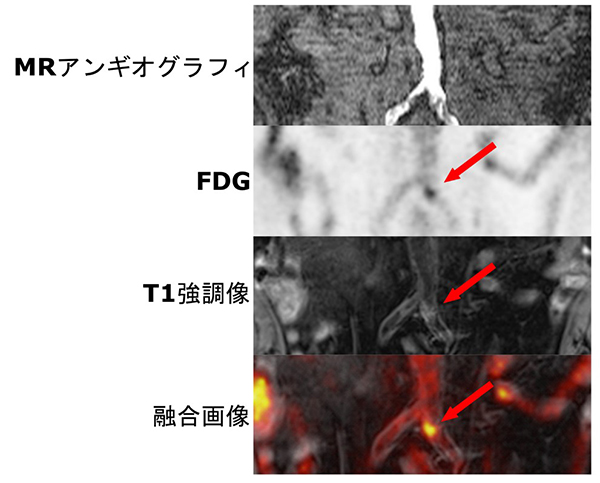 |
図3
両側腸骨動脈狭窄の症例です。MRアンギオグラフィでは両側の腸骨動脈ともに血管の狭窄を認めますが、FDGの集積は左腸骨動脈のみに認めます。MRIのT1強調像での高信号域はプラークの不安定性と関連していると報告されており、FDGの集積亢進はT1強調像での高信号域に一致しています。
|
13N-ammonia PET/MRIを用いた心筋血流量と心臓MRIの関連に関する研究
|
13N-ammoniaは心筋血流を評価可能なトレーサーで古くから心筋血流PETとして用いられてきました。13N-ammonia PETは2013年に本邦で保険適応となり、18F-FDG以外で臨床的に使用可能なトレーサーの一つです。高画質な定性的画像に加え、心筋血流の定量的な評価も可能となり、他枝病変の評価や微小循環の評価を行うことも可能です(図4)。PET/MRIを用いて13N-ammonia
PETを評価することで、これまでそれぞれ単独で評価されてきた心筋血流の情報とMRIの心筋の性状評価の対比、さらに負荷心筋血流PET撮像中のMRIの評価が可能となります。これにより、これまで報告されてきたPETやSPECTのQGSの精度をMRIと直接比較する検討や、心筋血流PETと心臓MRIの負荷パーフュージョンによる心筋血流定量との比較など、これまで明らかにするのが難しかった数多くの検討を行うことが可能です。
|
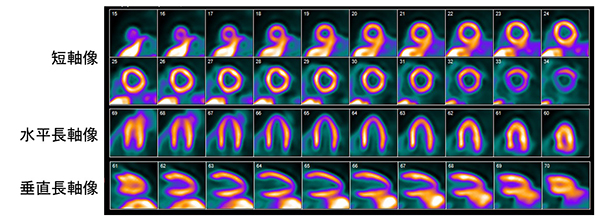 |
図4
冠動脈疾患のない患者のアンモニア定性画像です。各断面で、SPECTと比較して分解能の高い画像を得ることができます。
|
心筋血流SPECTの3D-OSEMを用いた再構成法に関する研究
|
| 心筋血流SPECTはFiltered back projectionによる再構成が一般的です。本研究では、逐次近似法の一つであるOSEM法による再構成法を用いることで、短時間収集の有効性を検討しています。当院では通常12分間の収集を行っていますが、6分間の短時間収集を追加し、画質の比較を行っています。また、実際に短時間収集の診断能の検討を行うことで、OSEM法の臨床への実用化を考えています。 |
これまでの主な業績
- Masuda A, Yamaki T, Kunii H, Nemoto A, Kubo H, Tominaga H, Oriuchi N, Takenoshita
S, Takeishi Y. Inflammatory involvement in a patient with Leriche syndrome
evaluated by 18F-fluorodeoxyglucose PET/MRI. J Nucl Cardiol. 2017;24: 1819-1821
- Takeishi Y, Masuda A, Kubo H, Tominaga H, Oriuchi N, Takenoshita S. Cardiac
imaging with 18F-fluorodeoxyglucose PET/MRI in hypertrophic cardiomyopathy. J Nucl Cardiol.
2017;24:1827-1828
- Masuda A, Manabe O, Oyama-Manabe N, Naya M, Obara M, Sakakibara M, Hirata
K, Yamada S, Naka T, Tsutsui H, Tamaki N. Cardiac fibroma with high 18F-FDG uptake mimicking malignant tumor. J Nucl Cardiol. 2017;24:323-324.
- Masuda A, Yamaki T, Sakamoto N, Kunii H, Ito H, Nanbu T, Kubo H, Hara T,
Takenoshita S, Takeishi Y. Vulnerable plaque on the common iliac artery
detected by 18F-fluorodeoxyglucose PET/MRI. Eur J Nucl Med Mol Imaging. 2016;43:793-794.
- Wada K, Niitsuma T, Yamaki T, Masuda A, Ito H, Kubo H, Hara T, Takenoshita
S, Takeishi Y. Simultaneous cardiac imaging to detect inflammation and
scar tissue with 18F-fluorodeoxyglucose PET/MRI in cardiac sarcoidosis. J Nucl Cardiol. 2016;23:1180-2.
- Masuda A, Takeishi Y. Choosing the appropriate examination for diagnosis
of stable ischemic heart disease. Ann Nucl Cardiol. 2016;2:167-173.
- Manabe O, Yoshinaga K, Ohira H, Masuda A, Sato T, Tsujino I, Yamada A,
Oyama-Manabe N, Hirata K, Nishimura M, Tamaki N. The effects of 18-h fasting
with low-carbohydrate diet preparation on suppressed physiological myocardial
18F-fluorodeoxyglucose (FDG) uptake and possible minimal effects of unfractionated
heparin use in patients with suspected cardiac involvement sarcoidosis.
J Nucl Cardiol. 2016;23:244-252.
- Masuda A, Yoshinaga K, Naya M, Manabe O, Yamada S, Iwano H, Okada T, Katoh
C, Takeishi Y, Tsutsui H, Tamaki N. Accelerated 99mTc-sestamibi clearance associated with mitochondrial dysfunction and regional
left ventricular dysfunction in reperfused myocardium in patients with
acute coronary syndrome. EJNMMI Res. 2016;6:41.
- Masuda A, Naya M, Manabe O, Magota K, Yoshinaga K, Tsutsui H, Tamaki N.
Administration of unfractionated heparin with prolonged fasting could reduce
physiological 18F-fluorodeoxyglucose uptake in the heart. Acta Radiol. 2016;57:661-668.
- Masuda A, Naya M, Yoshinaga K, Tamaki N. Imaging of myocardial innervation.
Nuclear Cardiac Imaging. Principles and Applications. Fifth edition. Ami
E Iskandrian, Ernest V Garcia, eds. USA, Oxford University Press. 2015:486-499.
|
|
