
- 深津 真彦(ふかつ・まさひこ)
- 医学部 血液内科学講座 助手

- 大河原 浩(おおかわら・ひろし)
- 医学部 血液内科学講座 博士研究員

- 王 新涛(おう・しんとう)
- 医学部 呼吸器内科学講座 博士研究員
- 研究グループ
- 深津真彦,大河原浩,王新涛,ロブナ・アルケブシ,古川未希,森博隆,深見美和,深見伸一,佐野隆浩,高橋裕志,原田佳代,木村哲,杉本浩一,小川一英,池添隆之
概要
論文掲載雑誌:「Science Signaling」(令和4年3月8日)
血液疾患の治療や造血幹細胞移植では,重症感染症や免疫応答に伴って,急性肺傷害 (ALI)/急性呼吸窮迫症候群 (ARDS) などの呼吸器合併症をしばしば発症します.しかし未だALI/ARDSには特異的治療法が確立されておらず,ときに致命的な経過を辿ります.
当研究グループはこれまで,Gas6というタンパク質とその受容体Merが,多発性骨髄腫の進行 (J Biol Chem. 2017;292:4280) や,造血幹細胞移植における血栓性微小血管症 (Blood Adv. 2009;3:2128) などに関与していることを報告してきました.そこで本研究では,ALI/ARDSにおけるGas6/Mer経路に着目した解析を行いました.
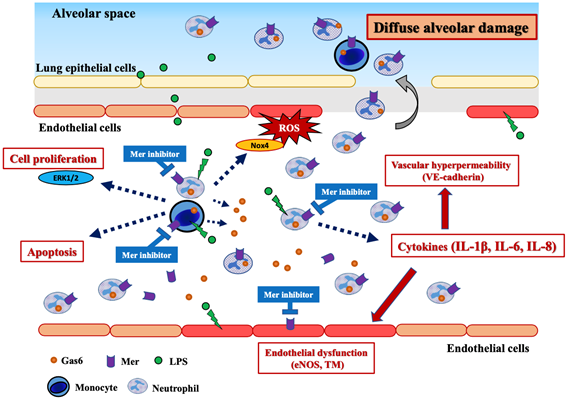
ALI/ARDSの動物モデルとして,マウスにリポ多糖 (LPS) を吸入させると,肺胞洗浄液中の炎症細胞の増加や,組織学的なびまん性肺胞傷害を示します.これらのモデルマウスでは血中Gas6の上昇を認めました.このモデルマウスにMerの阻害剤であるUNC2250を投与したところ,炎症細胞浸潤や肺胞傷害が抑制され,生存率が改善しました.培養細胞を用いてUNC2250の作用メカニズムをさらに検証すると,炎症細胞である好中球・マクロファージの増殖や,炎症性サイトカイン・活性酸素種の産生を抑制する効果に加えて,血管内皮の恒常性の維持に重要な分子の発現を保つ効果があることがわかりました.
実際に血液疾患の治療中にALI/ARDSを発症した患者の血中では,そうでない患者に比べて,Gas6と可溶性Merの濃度が上昇していました.以上のことから,Gas6/Mer経路は血液疾患に合併したALI/ARDSの治療標的となり,重篤な合併症を減らした安全な治療に寄与する可能性が示されました.
連絡先
公立大学法人福島県立医科大学 医学部 血液内科学講座
電話:024-547-1193
FAX:024-547-1194
講座ホームページ:https://www.hemato.fmu.ac.jp/
メールアドレス:hemato@fmu.ac.jp(スパムメール防止のため、一部全角表記しています)

