
- 近藤 悠斗 (こんどう・ゆうと)
- 先端臨床研究センター 助教
- 研究グループ
- 近藤 悠斗,木村 寛之,田中 万美子,服部 恭尚,河嶋 秀和,高橋 和弘,安井 裕之
概要
論文掲載雑誌:「The Journal of Organic Chemistry」(2025年6月11日)
放射性同位体(RI)を利用した分子イメージング技術は、臓器や組織の機能を非侵襲的に可視化できる技術として、基礎研究から臨床応用に至るまで広く活用されています。この技術を支えるRI標識プローブの設計と合成には、安定性と選択性に優れた標識法の確立が不可欠であり、標識法の多様化はいまなお重要な研究課題となっています。
本研究グループではこれまで、銅触媒を用いた脱ホウ素ヨウ素化(CuRIB)反応を基盤とする放射性ヨウ素標識法の開発に取り組んできました[1–4]。近年では、CuRIB反応とアジド–アルキン環化付加(CuAAC)反応を組み合わせることで、連続的な試薬添加と単回の精製工程のみで高効率にRI標識体を得ることができる、ワンポット標識法を確立しています[5]。しかしながら、この手法において、標識前駆体であるボロン酸化合物の合成が工程律速となり、候補化合物ライブラリーを迅速に展開するうえでの制約となっていました。そこで本研究では、ジオール樹脂を用いた固相合成法を新たに適用することでアリールボロン酸前駆体を樹脂上で効率的に構築し,それらをCuRIBおよびCuAAC反応を用いたワンポット標識法へ導入することで,前駆体合成から放射性標識までを効率的に一貫して行うことができる手法を新たに開発しました(図)。さらに,本研究では、医薬品に近い複雑な構造を有する分子、たとえばソマトスタチン受容体2(SSTR2)アンタゴニストであるペプチドLM3への適用も実証しており、本手法の高い応用性が示されています。
本手法は、RI標識プローブの合成を簡便化かつ高効率化する新たなプラットフォーム技術として、放射性医薬品の研究開発を加速させることが期待されます。さらに、この合成戦略は、当センターで現在推進しているアスタチン-211を用いた標的α線治療薬の開発にも応用が可能であり、次世代のα線を用いた放射線治療への展開も視野に入れています。今後は、より実用的なRI標識技術の構築を通じて、放射性診断薬・治療薬の新規開発に貢献してまいります。(近藤 悠斗)
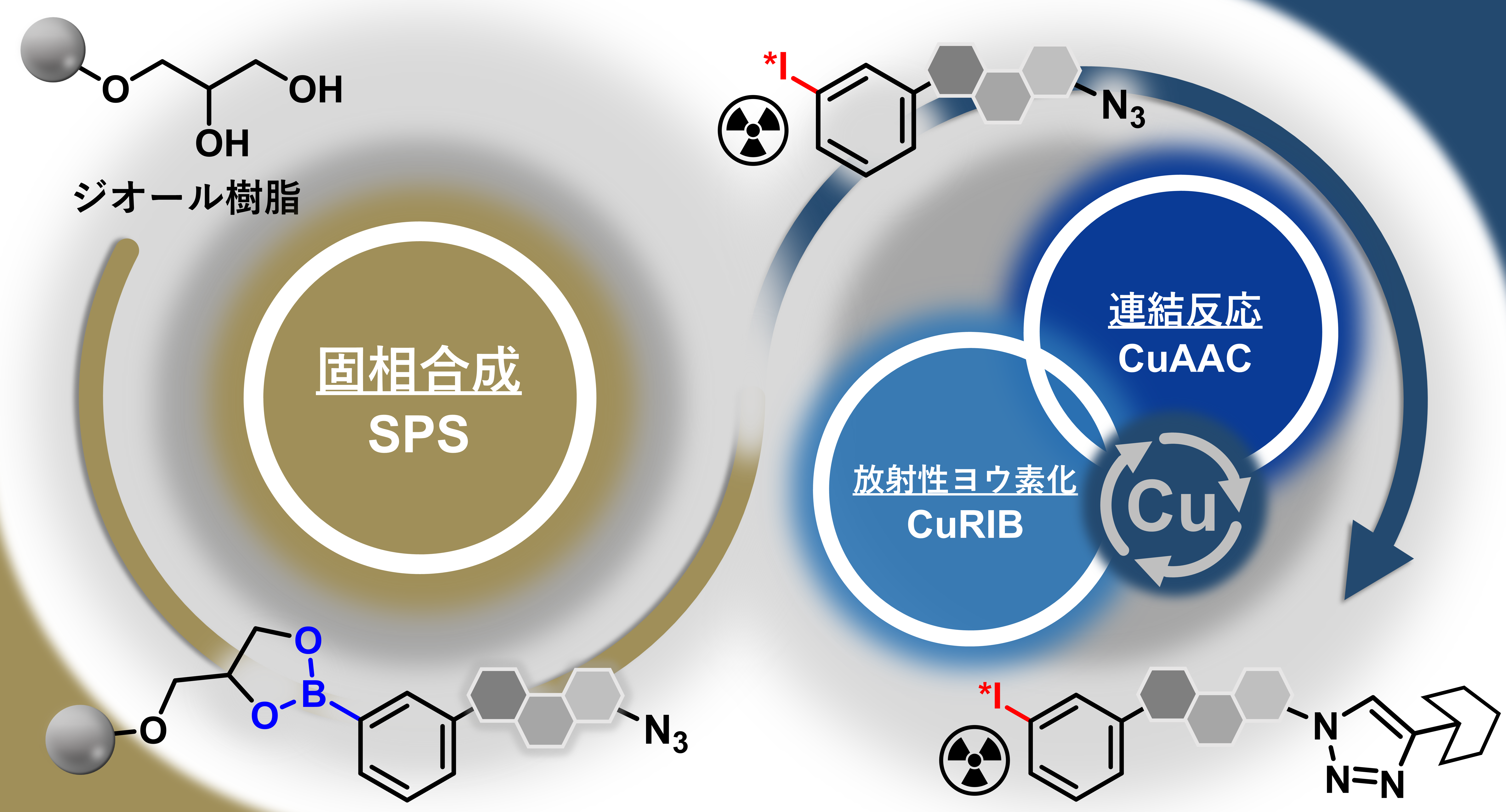
図:本手法の概要
参考文献
[1] Kondo, Y. et al., J. Labelled Compd. Radiopharm. 2021, 64, 336-345.
[2] Kondo, Y. et al., Bioorg. Med. Chem. 2022, 69, 116915.
[3] Kondo, Y. et al., ACS Omega 2023, 8, 24418-24425.
[4] Kondo, Y. et al., Chem. Eur. J. 2024, 30, e202403303.
[5] Kondo, Y. et al., Chem. Commun. 2024, 69, 714-717.
連絡先
公立大学法人福島県立医科大学 ふくしま国際医療科学センター 先端臨床研究センター
電話:024-581-5167
FAX:024-581-5170
講座ホームページ:https://www.fmu.ac.jp/home/acrc/

