知財
1.癌予後マーカー
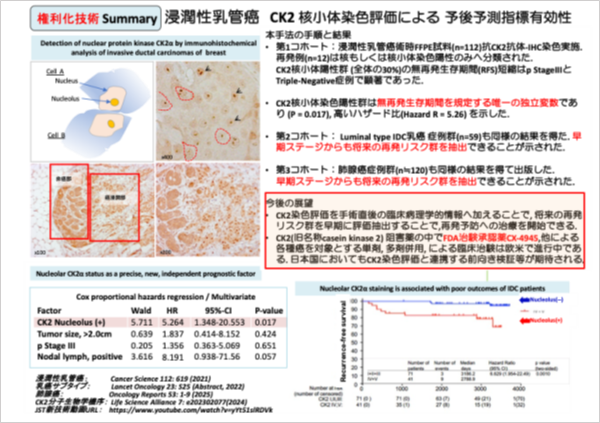
私たちは複数の固形癌を対象に、癌の早期ステージからも将来の再発リスクを予測する癌予後マーカー見出しました。それを基盤として、予後予測診断技術の社会実装を目標に開発を進めています。 対象とする分子CK2はリン酸化酵素として増殖関連酵素の一つですが、私たちは乳癌術時試料を用いた組織化学的手法による染色評価から、核の中の「核小体」におけるCK2分子集積 (核小体CK2染色陽性群)は将来の再発と関連することを初めて見出しました。様々な臨床データと照合する統計解析の結果、核小体CK2染色陽性は予後について最も寄与率が高いマーカーであり、統計学的にも「将来の無再発生存期間を規定する独立変数である」事を明らかにしました。10年フォローしたコホート解析の結果、それらの核小体陽性群は陰性群と比較し時間経過とともに再発しやすいグループであることが示されました。癌手術時の検体もしくはそれ以前に診断用として癌部から取出す小さな針生検体を調べることで、再発するまで待つ事なく、再発リスクある方を早期に見出すことができると期待されます。また近年の解析から、核小体CK2染色評価手法は、治療薬剤への抵抗性ある集団をあらかじめ予測可能なマーカーとしての有効性も示唆されました。
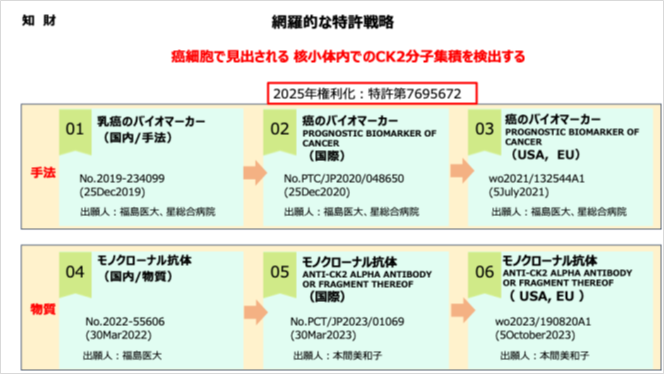
この背景にあるのは、細胞増殖に伴い、CK2の一部が核内に入ることを見出した基礎研究の結果です。CK2分子は、正常細胞においては主に細胞質に局在しているのですが、浸潤性乳管癌、肺腺癌の手術検体を対象としてCK2抗体による組織染色評価を行った結果、およそ95%の症例で細胞核内でのCK2レベルの上昇があること、さらに30%の症例で核の中の核小体へ集積すること、核小体へのCK2集積は、正常とは異なる癌浸潤部でのみ見出されること、を明らかにしました。個々人の癌を詳しく調べるための検査としては、ゲノム変異の解析や、遺伝子もしくはタンパク質発現量の変化を、正常組織と対比し判定する手法が主流です。一方、本手法は特定分子(CK2)の細胞内局在変化を見出す新たな視点に立つ発見(細胞質に局在する分子が核小体へ集積する)であり、さらに統計解析によって精度の高い予後マーカーである検証を経て、本手法は2025年6月に国内権利化されました。
個体における癌再発には初発部位局所での再発と、血液やリンパ等の脈管系を経由して遠隔組織へ転移する再発があり、それら分子メカニズムを解明することは癌克服のために大きな課題となっています。近年、私たちは分子生物学的手法を用いてCK2が細胞周期進行の増殖期に伴い核や核小体にあるゲノム上にリクルートされることを見出し、再構成実験系によってターゲット遺伝子群の研究を進めています。核小体は細胞の司令塔として重要な役割を担うと考えられていますので、癌化もしくは癌悪性化に伴うシグナル軸等、分子機序の詳細を明らかにしたいと考えて研究を進めています。
| 癌予後マーカー(権利化知財) 概要 | PDF①,PDF② |
|---|---|
| 浸潤性乳管癌(IDC)を対象とした研究 そのサブタイプ(Luminal) へ絞った解析 |
|
| 肺腺癌を対象とした研究 | |
| 核内CK2機能の分子生物学的研究 | |
| 細胞周期進行におけるCK2の役割 | PDF①,PDF② |
| CK2総説(日本生化学会誌) | |
| 研究紹介 | PDF①,PDF② |
| 癌ドライバー遺伝子(変異型PKA)についての研究 | |
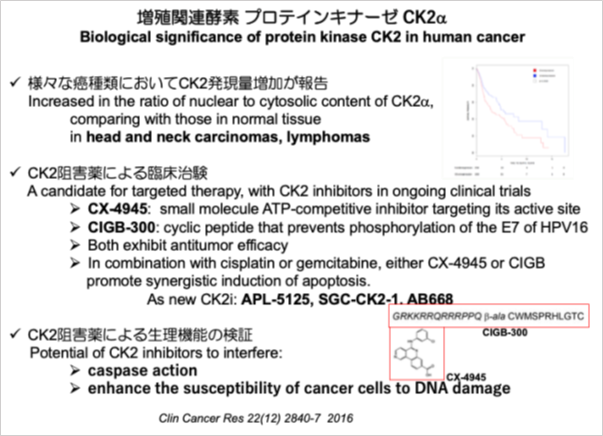
| FDA治験承認薬: CK2に対する低分子阻害薬 | |
| JST新技術発表会 |
|
| みちのくアカデミアスタートアップplatform:採択課題 |
|
2. ミトコンドリア機能と関連する阻害薬の開発
ミトコンドリアは、エネルギー産生を担う細胞内小器官のひとつですが、機能異常により神経変性疾患や癌をはじめとして様々な加齢性疾患の発症に関わることが知られています。私たちは、ミトコンドリア機能制御機構の解析を通して、細胞性粘菌の二次代謝産物の中から、生理活性を有するプレニルオキシキノリンカルボン酸誘導体(PQA)を同定しました。
ムラサキカビモドキ属((Polyshondylium pseudo-candidum)に由来するPQA化合物の一つであるPpc-1は、生化学解析の結果、ミトコンドリア酸素消費を増加させる作用が見出され、マウス個体における体重の増加を抑制することから代謝改善薬としての応用が期待されます。また、Ppc-1を基に側鎖構造の異なる約20種のPQA化合物を合成しました。その中のPQA-18は、免疫細胞におけるインターロイキン2をはじめとするサイトカイン産生の抑制作用を示し、マウス個体における免疫応答を抑制しました。プロテオーム解析および放射標識ATPを用いたin vitroキナーゼアッセイを行い、PQA18がp21-activated kinase 2(PAK2)の阻害薬であることを見出しました。さらに、アトピー性皮膚炎モデルマウスを用いた解析を行い、PQA18軟膏が皮膚炎の症状を改善させました。これらの結果からPQA18はPAK2阻害を機序とする免疫抑制薬であり新規のアトピー性皮膚炎治療薬としての応用が期待されます。一方、PQA-11は、グルタミン酸やアミロイドβによる培養神経細胞死を抑制しました。シグナル解析の結果から、アポトーシスシグナル分子であるmitogen-activated protein kinase kinase 4を阻害することが明らかとなりました。MPTP誘導性パーキンソン病モデルマウスにおけるPQA11の投与によって、黒質のドパミン神経細胞死が抑制されることから新規の神経変性疾患改善薬としての応用が期待されます。
神経変性疾患においては、部位特異的な神経細胞死が観察されるのみならず、周囲のグリア細胞の活性化が起き神経炎症が惹起されていることが知られています。PQA11の投与によって神経細胞死を抑制できるのですが、完全なものではありませんでした。また、PQA11だけでは、グリア細胞の活性化を抑制することはできませんでした。このことから、脳内炎症を抑制するためグリア細胞の活性化を抑制する低分子化合物の探索を行っています。
特許
本間好、鈴木俊幸、小椋正人、大島吉輝、菊池晴久
プレニルオキシキノリンカルボン酸誘導体
出願番号PCT/JP2013/077937 (2013年10月15日)
大島吉輝、菊池晴久、本間好、鈴木俊幸、小椋正人
体重増加制御剤
特許特願2012-230985号、(2012年10月18日)

