木下 専(名古屋大学)

「嗅内皮質-海馬歯状回シナプス分子欠乏による空間失認と適応的代償機構の解析」
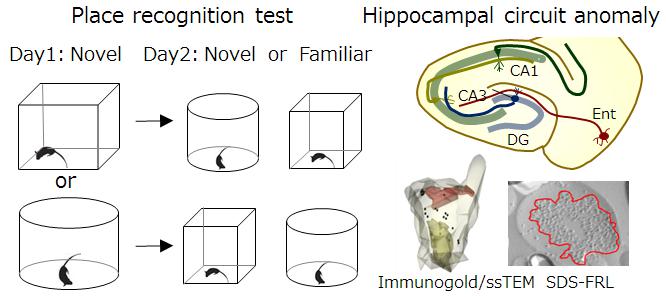
嗅内皮質―海馬間の双方向性興奮性投射路が構成する閉鎖回路は記憶と空間認知の中枢として重要である。興奮性シナプスの近傍(pre/post/
perisynapse)には足場蛋白質セプチン(SEPT1-14)のサブセットから成る線維状重合体が局在してシナプス伝達調節に寄与しているが(2007, 2013, 2015)、postsynapseにおける機能は全く不明である。当グループは、特定のセプチン・サブユニットを欠損する遺伝子改変マウス系統が空間定位や空間記憶を維持しながらも空間形状の弁別能力を欠くことを一連の行動学的試験により見出した。ヒトにおいては認知症や統合失調症などの部分症状として生じる空間失見当識が深刻な問題となる。そこで上記系統が呈するユニークな認知機能障害の責任領域を精査したところ、上記神経回路の特定のシナプスにおける後シナプス膜上グルタミン酸受容体の欠乏とスパインの未熟化を認め、限局的なシナプス伝達障害が示唆された。しかし、発生期からの慢性的セプチン欠損に対して類似遺伝子が発現変動するなどして異常が代償されている可能性も示唆された。そこで当該シナプスのセプチンを細胞選択的かつ急性に欠乏/欠損させる分子レベルのlesion studyを行い、行動>シナプス微細構造>シナプス分子の3つの階層でフェノタイプを精査する。即ち、1)セプチン急性欠乏によるシナプス阻害により、上記マウスの空間弁別障害の責任シナプスの確定と適応的代償メカニズムの探索を行う。2)セプチン重合の要となる必須サブユニットSEPT7の局所的急性欠損によるシナプス阻害で上記マウスより重度の空間失見当識モデルを作り、この系を活用してシナプス~回路の破綻の病態生理と適応的代償メカニズムを詳細に解析する。空間失見当識の動物モデルを開発・解析し、シナプス分子レベルで発症と代償性回復メカニズムの理解を目指す。
最近の主要論文
1. Ageta-Ishihara N, Kinoshita M et al., A CDC42EP4/septin-based perisynaptic glial scaffold facilitates glutamate clearance. Nature Communications 6:10090, 2015.
2. Hattori Y, Kinoshita M, Ihara M et al., SIRT1 counters cerebral hypoperfusion injury by deacetylating eNOS. Stroke 45, 3403-3411, 2014.
3. Ageta-Ishihara N, Bito H, Kinoshita M et al., Septins promote dendrite and axon development by negatively regulating microtubule stability via HDAC6-mediated deacetylation. Nature Communications 4, 2532, 2013.
4 Ageta-Ishihara N, Kinoshita M et al., Chronic overload of SEPT4, a parkin substrate that aggregates in Parkinson’s disease, causes behavioral alterations but not neurodegeneration in mice. Molecular Brain 6, 35, 2013.
5. Ihara M, Kinoshita M et al. Sept4, a component of presynaptic scaffold and Lewy bodies, is required for the suppression of α-synuclein neurotoxicity. Neuron 53, 519-533, 2007.
投稿日:2015年12月20日