木下 専(名古屋大学)

「嗅内皮質-海馬歯状回シナプス機能不全による空間弁別障害と適応的代償機構の解析」
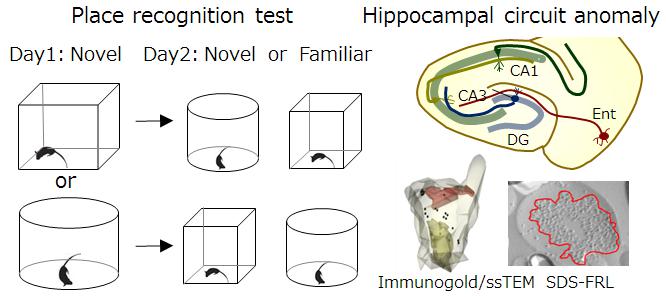
空間認知・記憶を担う海馬神経回路のうち、嗅内皮質(貫通線維)から海馬歯状回(顆粒細胞)への投射 (pp-GC)は発火閾値が高く、sparse codingによるパターン分離(空間文脈の弁別)に重要とされている。このユニークなグルタミン酸作動性シナプスの樹状突起棘(スパイン)には重合性GTPaseセプチンの複数のサブユニットが局在するが、生理的意義は不明である。我々は、そのうちの1サブユニットを欠損するマウスの空間定位・記憶が正常であるにもかかわらず、形状の異なる空間文脈を混同することを見出した。空間弁別障害モデルとして精査したところ、海馬の主要シナプスの中ではpp-GCでのみ選択的シナプス伝達・成熟障害を示唆する所見が得られた。本領域前期では、1) 野生型マウス顆粒細胞のRNAiによるセプチン欠乏が空間弁別障害の再現に必要であり、2) 欠損マウス顆粒細胞へのセプチン補充が認知障害のレスキューに十分であることを示すことで、空間弁別障害の責任シナプス(ニューロン)を絞り込むことに成功した。後期には、セプチンの欠乏ないし欠損からシナプス機能障害に至るメカニズムの解明を目指して、蛍光ライブイメージング、神経薬理学的操作、プロテオミクスを組み合わせた探索を進める。さらに、セプチン重合の要となる必須サブユニットを顆粒細胞選択的に欠乏・欠損させ、より重度の空間弁別障害モデルマウスの作製を試み、機能破綻と適応的代償メカニズムを解析する。行動>海馬神経回路>シナプス活動>シナプス微細構造>シナプス分子の階層での異常を詳細に精査することを通じて、認知症や統合失調症などの精神・神経疾患の部分症状として頻度の高い空間見当識障害の病態理解につながることも期待される。
最近の主要論文
1. Ageta-Ishihara N, Kinoshita M et al., A CDC42EP4/septin-based perisynaptic glial scaffold facilitates glutamate clearance. Nature Communications 6:10090, 2015.
2. Hattori Y, Kinoshita M, Ihara M et al., SIRT1 counters cerebral hypoperfusion injury by deacetylating eNOS. Stroke 45, 3403-3411, 2014.
3. Ageta-Ishihara N, Bito H, Kinoshita M et al., Septins promote dendrite and axon development by negatively regulating microtubule stability via HDAC6-mediated deacetylation. Nature Communications 4, 2532, 2013.
4 Ageta-Ishihara N, Kinoshita M et al., Chronic overload of SEPT4, a parkin substrate that aggregates in Parkinson’s disease, causes behavioral alterations but not neurodegeneration in mice. Molecular Brain 6, 35, 2013.
5. Ihara M, Kinoshita M et al. Sept4, a component of presynaptic scaffold and Lewy bodies, is required for the suppression of α-synuclein neurotoxicity. Neuron 53, 519-533, 2007.
投稿日:2017年05月08日